1 영양소의 특성
1-1. 개요
비타민 E는 항산화기능을 갖는 영양소로 천연에는 α-, β-, γ-, δ- 토코페롤(tocopherol)과 α-, β-, γ-, δ- 토코트리에놀(tocotrienol) 형태로 존재한다. 아래 그림과 같이 토코페롤은 고리구조와 탄소로 된 긴 포 화측쇄로 되어 있으며, 토코트리에놀은 불포화측쇄를 가진다 [1]. 이들 비타민 E의 생리적 활성은 α-토코 페롤이 가장 크고, β-, γ-, δ-토코페롤의 경우에는 α-토코페롤 수송 단백질(α-tocopherol transfer protein, α-TTP)에 대한 친화력이 상대적으로 매우 낮고 체내에서 α-토코페롤로 전환되지 않는 것으로 보 고 되었다 [2]. 이와 같은 근거를 바탕으로 미국, 일본 등에서는 비타민 E 권장량 설정 시 α-토코페롤만을 활성 비타민 E로 간주하고 있으나 [2], 우리나라에서는 8개의 비타민 E를 모두 활성 비타민 E 로 간주하고 생체역가를 계산하여 α-토코페롤 당량(α-TE)로 권장량을 표시한다.

또한 구조적으로 α-토코페롤은 2,4,8 위치에 비대칭 탄소를 가지고 있어 4개의 2R-입체이성체(RRR-, RSR-, RRS-, RSS-α-토코페롤)와 4개의 2S-입체이성체(SRR-, SSR-, SRS-, SSS-α-토코페롤)로 총 8개의 입체이성체가 가능하다 [3]. 그런데 이들 8개의 입체이성체 중 자연에서 유래하는 α-토코페롤은 RRR-α-토코페 롤 형태로만 존재하며, 그 외 7개의 입체이성체는 비타민 강화식품이나 보충제 등의 합성 α-토코페롤에만 존재한다. 자연형 α-토코페롤은 RRR-α-토코페롤 또는 d-α-토코페롤로 표기되어 왔으며, 합성형 α-토코페 롤의 경우 all-rac-α-토코페롤 또는 dl-α-토코페롤로 표기되어 왔다.
8개의 α-토코페롤 입체이성체중에서 쥐를 이용한 동물실험에서 RRR-α-토코페롤이 가장 큰 생리적 활 성을 나타내었으며, 그 외의 2R-입체이성체는 일반적으로 2S-입체이성체에 비해 활성이 큰 것으로 나타났 다 [4, 5]. 또한 α-토코페롤의 2S-입성이성체는 인체의 혈액 [6]이나 조직 [7]에 보유되지 않는 것으로 보고 되었다. 이와 같은 과학적인 근거를 바탕으로 미국에서는 비타민 E의 권장량 설정시에 α-토코페롤의 2R- 입성이성체만을 활성 비타민 E로 간주하고 있으며, 2016년에 자연형 α-토코페롤인 RRR-α-토코페롤과 합 성형 α-토코페롤인 all-rac-α-토코페롤의 생체역가(biopotency) 비율을 1.36:1에서 2:1로 변경하여 보충제 라벨에 표시하기로 결정하였다 [8].
1-2. 흡수, 분포, 대사, 배설
비타민 E는 지방, 담즙염과 함께 미셀(micelle)을 형성하여 소장 상부에서 흡수된다. 보충제에 함유된 토코페롤은 대부분 아세테이트(acetate)나 숙신산(succinate)과 같은 지방산 에스테르 형태이다. 따라서 보 충제로 섭취하는 비타민 E는 췌장의 에스터가수분해효소(esterase)에 의하여 가수분해 되어야 흡수될 수 있다. 비타민 E의 흡수는 20-80% 정도로 그 폭이 크며 평균적으로 30-50%로 보고되었다 [9-11]. 비타민 E의 흡수는 지방 섭취량이 증가하면 높아지고 지방이 없는 상태에서는 약 10%의 흡수율을 보이는 것으로 알려져 있다 [11]. 그러나 건강한 여성을 대상으로 α-토코페롤에 2개의 중수소 표시(2 deuterium-labeled) 를 하여 수행한 비교적 최근의 연구에 따르면 비타민 E의 흡수는 지방의 유무와는 관련이 없고 유미지립 (chylomiron) 형성 과정에 의존한다고 보고되었다 [12]. 비타민 E의 형태에 따른 흡수율의 차이도 연구되 었는데 γ-토코페롤이 α-토코페롤의 85% 수준이라는 보고가 있지만 [13] 그 외 다른 형태의 토코페롤의 흡수에 대한 자료는 제한적이다. 일반적으로 비타민 E 보충제 등을 과량 섭취하게 되면 흡수율이 감소하는 것으로 알려져 있다 [14].
비타민 E의 수송은 혈청 지단백질이 담당하게 되며 흡수 후에는 유미지립(chylomicron)이 주된 역할을 하지만 모든 지단백질이 관여하게 된다. 혈액 내 비타민 E는 저밀도지단백질(low density lipoprotein, LDL)에 약 65%, 고밀도지단백질(high density lipoprotein, HDL)에 약 24%, 그리고 초저밀도지단백질 (very low density lipoprotein, VLDL)에 약 8% 정도로 존재한다. 혈액에서 유미지립에 존재하는 비타민 E는 고밀도지단백질로 이동하기도 하고 또 다른 혈청 지단백질로 이동하기도 한다. 그러나 지단백질리파 아제(lipoprotein lipase, LPL)에 의하여 유미지립 내의 지방이 분해되어 조직으로 유입될 때 유미지립에 존재하던 비타민 E가 조직으로 함께 수송되기도 한다. 이렇게 비타민 E가 유입되는 조직은 근육과 지방조 직 및 뇌 조직 등 지단백질리파아제가 존재하는 조직에 해당하며 식사에서 섭취한 모든 형태의 비타민 E가 유입될 수 있다. 유미지립 잔여물질이 간으로 유입될 때에는 유미지립 잔여물질에 함유된 비타민 E도 같이간으로 유입되게 되는데 그 양이 섭취한 비타민 E의 상당 부분을 차지한다. 간으로 유입된 비타민 E는 간 에서 생성되는 초저밀도지단백질에 함유되어 혈액으로 나오게 되고 역시 지단백질리파아제의 작용을 받은 후 저밀도지단백질에도 남아 있다가 간 외 조직으로 유입되기도 하고 고밀도지단백질로 이동하기도 한다 [15]. 비타민 E는 이렇게 여러 지단백질 사이에서 교환될 뿐 아니라 적혈구와도 빠르게 교환되어 적혈구의 산화적 용혈을 억제한다.
간에서 혈액으로 방출된 초저밀도지단백질 내에 함유된 비타민 E는 주로 α-토코페롤이라고 알려져 있 다. 이는 간 세포 내에서 초저밀도지단백질이 합성될 때 8가지 형태의 비타민 E중에서 α-토코페롤이 우선 적으로 유입 될 뿐 만 아니라 간 세포에 존재하는 α-토코페롤 수송 단백질(α-TTP)이 α-토코페롤만을 선택 적으로 운반하는 것으로 알려져 있다 [16, 17]. 다른 형태의 비타민 E는 α-토코페롤 수송 단백질에 대해 친화력이 매우 낮은 것으로 보고되었다. α-토코페롤 수송 단백질에 대한 α-토코페롤의 친화력을 100으로 본다면 β-토코페롤은 38, γ-토코페롤은 9, δ-토코페롤은 2(이상은 모두 RRR 형), SRR-α-토코페롤은 11, α-토코트리에놀은 12 이었다 [18]. 혈액의 비타민 E 농도는 간에서 나오는 비타민 E에 의해 결정되며, 간 에서 α-토코페롤이 선택적으로 분비된다는 것은 주목할 만하다 [6]. α-토코페롤 수송 단백질 외에도 토코 페롤과 결합하는 단백질로 세포 레틴알데히드 결합 단백질(cellular retinaldehyde binding protein) [19]과 토코페롤 결합 단백질 [20]이 간 조직을 포함한 여러 조직(심장, 뇌, 소장세포)에 존재하는 것으로 알려져 있으나 이들 단백질의 기능과 생리적 활성에 대하여 더 많은 연구가 필요한 실정이다.
라디칼 포획자(radical scavenger)인 α-토코페롤이 체내에서 독성이 강한 산화물질인 토코페록실 라디 칼(tocopheroxyl radical)로 전환되면 비타민 C와 글루타티온계에 의하여 재생될 수 있다. 토코페롤로 재 생되지 못한 토코페록실 라디칼은 토코페릴 퀴논(tocopheryl quinone)으로 전환된 후 글루쿠론산과 포합 하여 대변으로 배설된다. 또한 섭취한 비타민 E의 약 1% 정도는 α-토코페론산(α-tocopheronic acid)과 α-토코페로노락톤(α-tocopheronolactone)으로 전환되어 소변으로 배설된다 [21]. α-토코페롤의 섭취가 많 아져 혈중 농도가 30 μmol/L(1,290 μg/dL)을 초과하게 되면 소변으로 2,5,7,8-tetramethyl-2-(2’-carboxy- ethyl)-6-hydroxychroman(α-CEHC)의 배설이 증가하는 것으로 알려졌으며 [22], 혈장 γ-토코페롤 농도를 감소시키는 것으로 보고되었다 [23]. 그러나 α-CEHC 대사물은 α-토코페롤 섭취량의 미미한 부분이므로 α-CEHC 배설은 α-토코페롤 필요량 평가에 이용되지 않는다.
1-3. 기능
비타민 E의 체내 기능은 항산화 작용과 그 외 생리적 기능으로 구분될 수 있다. 항산화작용은 자유라디 칼(free radical)의 연쇄반응을 차단하여 산화적 스트레스를 억제하는 것이다. 비타민 E는 주로 세포막과 지단백질 표면에서 작용하게 되는데 이들을 구성하는 인지질의 다불포화지방산(polyunsaturated fatty acid, PUFA)에서 생성되는 페록실 라디칼을 제거하는 역할을 한다. 비타민 E는 항산화 기능의 효율이 높 기 때문에 세포막에 존재하는 비타민 E와 다불포화지방산의 비율이 낮더라도 세포막에 존재하는 다불포화 지방산의 산화를 억제하여 세포막을 잘 보호할 수 있다. 이와 같이 비타민 E가 항산화제로서 높은 효율을 가질 수 있는 이유는 비타민 E가 글루타티온(glutathione)과 비타민 C의 도움으로 라디칼 형태에서 원래상 태로 빠르게 돌아올 수 있는 재생기전 때문이며, 비타민 E의 turnover 또한 매우 느리기 때문이다 [15].
비타민 E의 형태에 따라 항산화반응 기전이 다른데 γ-토코페롤은 α-토코페롤에 비하여 활성산소 라디칼과의 반응도는 낮으나 [24] 과산화질산염(peroxynitrite)과 같은 활성질소 라디칼과 반응하여 5-nitro-γ-토코페롤을 생성함으로서 [25] 조직성분을 보호하고 항염증 작용에 관여한다. 비타민 E는 민무늬 근육, 혈 소판, 단핵구 등에서 단백질 인산화효소 C(protein kinase C, PKC)의 활성을 저해하는 것으로 보고되었다. 뿐만 아니라 비타민 E는 단핵구가 혈관 내피세포에 부착되는 것을 억제하는데, 이는 혈관내피 세포에서 세포간부착분자(Intercellular Adhesion Molecule-1, ICAM-1), 혈관세포부착분자(Vascular Cell Adhesion Molecule-1, VCAM-1)과 같은 세포부착분자(cell adhesion molecule)의 발현을 억제함으로써 가능한 것으로 알려졌다. 또한 비타민 E는 5-리폭시게나아제(5-lipoxygenase)와 사이클로옥시게나아제 -2(cyclooxygenase-2)의 활성을 억제하여 염증을 촉진하는 IL-1β, IL-8 등의 사이토카인(cytokine) 및 플 라스미노겐 활성화인자억제제-1(plasminogen activator inhibitor-1)과 C-반응성 단백질(C-reactive protein)의 분비도 억제한다 [15]. 이와 같은 비타민 E의 생화학적 작용은 주로 α-토코페롤을 사용하여 조 직 배양이나 ex vivo 연구를 통해 이루어졌다.
α-토코페롤 이외 다른 형태의 비타민 E에 대한 연구도 이루어졌는데 Jiang 등 [26]은 γ-토코페롤과 그 대사물인 γ-carboxyethyl hydroxychroman(CEHC)도 대식세포 내의 사이클로옥시게나아제-2(cyclooxygenase-2, COX-2)의 활성을 억제하며 그 효과가 α-토코페롤보다 더 좋았다고 보고하였다. 이 들은 또한 다른 형태의 비타민 E를 이용한 동물실험에서 α-토코페롤 섭취와 비교하였을 때, γ-토코페롤 섭취 시에 프로스타글란딘(prostaglandin) E2 양이 염증 부위에서 더 감소되었고 총 질산염/아질산염 (nitrates/nitrite) 양과 8-isoprostanes 및 종양괴사인자(tumor necrosis factor)의 생성이 낮아진 결과를 얻 음으로써 염증 억제에 상당한 효과가 있다고 결론지었다 [27]. 그러나 토코페롤의 여러 형태, 특히 α-토코 페롤과 비교한 γ-토코페롤의 생화학적 기능에 대한 효과와 인체에서의 영향에 대한 비교 연구가 더 필요 하다고 할 수 있다.
2 건강 유지 및 증진을 위한 섭취기준
2-1. 건강을 위한 섭취기준 설정 시 고려사항
비타민 E의 섭취기준을 선정하기 위한 주요 질문은 비타민 E의 용혈작용에 대한 효과, 산화적 스트레스 에 대한 효과, 비타민 E 섭취와 혈액 농도와의 관련성, 그리고 심혈관계질환, 암, 면역계질환, 중추신경계 질환 등에 대한 효과, 그리고 비타민 E의 지방산화 억제 및 비타민 과다섭취에 따른 부작용 등이었다. 영 양상태의 반영지표는 자연식품에서 섭취할 수 있는 α-토코페롤과 비타민 E 보충제 및 강화제에 존재하는 합성 α-토코페롤을 포함하는 α-토코페롤 당량이었다.

2-1-1. 섭취기준 설정을 위한 지표의 선정
인체에 비타민 E가 필수 영양소인 것은 알려져 있으나, 최근 우리나라에서는 명백한 비타민 E 결핍 증 세를 보이는 사람은 없는 실정으로 한국인의 식생활 형태가 비타민 E를 충분히 제공하는 것으로 보인다. 그런데 한국인의 비타민 E 영양 상태는 섭취량만 조사되어 있고, 혈액의 비타민 E 형태별 농도에 대한 연 구는 거의 없는 실정이다. 뿐 만 아니라 비타민 E 섭취량 평가의 정확성에 있어서도 합성비타민 및 자연비 타민의 혼재, 다양한 비타민 E의 형태 등에 의해 정확한 비타민 E 섭취량의 평가에 어려움이 있다. 이와 같은 제한된 자료를 가지고 비타민 E의 섭취기준을 설정하는 데는 어려움이 있다고 할 수 있다. 따라서 비타민 E의 섭취기준 설정을 위한 지표로는 현재까지 가장 과학적인 자료로 받아들여지는 적혈구 용혈작 용과 혈액 내 비타민 E 농도를 이용하였다.
2-1-2. 필요량 추정에 사용될 수 있는 지표
(1) 혈액 α-토코페롤 농도
비타민 E의 섭취량과 혈장 비타민 E의 농도와의 연관성은 다양하게 나타났다. 일상식을 통해 섭취한 비타민 E의 경우 혈액 비타민 E 농도와 관련성이 없는 반면 [28], 보충제로 섭취할 경우에는 혈액 비타민 E 농도와 연관성이 있는 것으로 보고되었다 [29, 30]. 미국 국민건강영양조사(NHANES III) 자료 분석 결 과 24시간 회상법으로 측정한 비타민 E 섭취량은 혈장 비타민 E 농도와 상관성을 보이지 않았다 [31]. 그 러나 비타민 E 결핍을 유도한 사람에게 α-토코페롤 아세테이트를 단계별로 증가시켰을 때 혈장 α-토코페 롤 농도가 그에 비례하여 증가하였다 [32].
(2) 과산화수소 유도 용혈반응
비타민 E가 결핍된 아동들에 있어서 혈장 α-토코페롤 농도는 과산화수소로 유도된 용혈반응과 반비례 함이 보고된 바 있다 [33]. 현재로서는 섭취량에 따른 혈장 농도와 과산화수소로 유도된 용혈반응의 연관 성을 평균필요량의 결정 기준으로 활용하는 것이 일반적으로 받아들여지고 있다. 그러나 정상인에게서 비 타민 E 섭취량에 따른 혈장 농도 변화가 민감하지 않아 [31] 비타민 E 섭취량(혈장 농도)으로 생체 내 과산 화수소로 유도된 용혈반응을 추적하기는 쉽지 않다. 이러한 연구는 1960년대 초반에 이루어진 성인 남자 대상의 Horwitt의 연구 [34]가 유일하다. 이 연구에서 연구대상자들을 장기간에 걸쳐 체내 비타민 E를 고 갈시킨 후 자연 토코페롤 아세테이트 또는 합성 토코페롤 아세테이트를 7.5 mg에서 320 mg까지 단계적으 로 공급한 후 혈액의 α-토코페롤 농도를 측정하고 과산화수소로 유도된 용혈반응을 측정하였다. 그 결과 는 α-토코페롤 아세테이트의 섭취가 60 mg(α-토코페롤 57.7 mg)에 이를 때까지 혈액의 α-토코페롤 농도 가 지속적으로 증가하였다. 또한 혈액의 α-토코페롤 농도가 12 μmol/L이상인 대조군(6명)에서는 과산화 수소로 유도된 용혈반응이 12% 미만이었지만, 혈액의 α-토코페롤 농도가 평균 12 μmol/L내외인 비타민 E 고갈군(4명)에서는 용혈반응이 80%로 매우 높았다. 혈액의 α-토코페롤 농도를 12 μmol/L 이상으로 유 지할 수 있는 α-토코페롤의 적정 섭취량을 찾기는 어려우나 미국에서는 섭취량과 혈액의 비타민 E 농도의 관련성을 회귀분석하여 평균필요량을 12 mg 으로 산정하였다 [2].
(3) 지질과산화지표
비타민 E 결핍으로 발생하는 대표적인 임상증상은 세포막 지질의 과산화 촉진이라고 할 수 있다. 따라 서 지질과산화 생물지표인 혈장이나 소변의 thiobarbituric acid reactive substances(TBARS), 말론디알데 히드(malondialdehyde), conjugated diene, F2-이소프로스탄(F2-isoprostane) 및 호흡에서 호기 중의 펜 테인(pentane), 에테인(ethane) 등이 비타민 E 부족 평가의 지표로서 고려된 바 있다. 그러나 이 물질들의 농도 변화는 비타민 E의 섭취뿐만 아니라 항산화영양소 및 인체의 전반적인 산화 환원 상태와 연관이 되므 로 비타민 E 섭취기준을 결정하는 데는 이용되지 않고 있다.
(4) 비타민 E 대사물질 배설
비타민 E의 대사물인 carboxyethyl-hydroxychroman(CEHC)의 배설을 측정하는 것도 제안되었으나 [35], 비타민 E 섭취량에 비하여 CEHC의 체내 함량이 매우 적어 필요량 추정에 실질적인 지표가 되기에는 제한점이 있다.
2-1-3. 필요량에 영향을 주는 요인
항산화 비타민인 비타민 E의 필요량은 체내에서 산화되기 쉬운 다불포화지방산(PUFA)의 섭취량과 밀접 한 연관성을 가진다고 할 수 있다. 서구에서는 다불포화지방산 섭취량에 대한 비타민 E의 적합한 섭취 비 율로 최소 0.4-0.6 mg α-토코페롤/g PUFA가 제안된 바 있다 [36]. 그러나 우리나라에서는 서구에 비해 불포화도가 높은 n-3계 리놀렌산(linolenic acid), 에이코사펜타에노산(eicosapentaenoic acid, EPA) 도코 사헥사엔산(docosahexaenoic acid, DHA)의 섭취가 더 높을 수 있으므로 총 다불포화지방 섭취에 대한 비타민 E 비율의 상향조절을 고려할 필요가 있다 하겠다. 비타민 E의 재생에 관여하는 그 외 항산화 영양 소인 비타민 C, 셀레늄 등 과의 정량적인 관계는 고려되지 않았다.
2-1-4. 섭취 부족 시 나타나는 건강문제
비타민 E 섭취 부족 시 나타나는 체내 증상의 경우 사람에게서는 거의 발견되지 않았다. 비타민 E의 영양상태는 혈청 α-토코페롤 농도를 기준으로 0.5 mg/dL 이상이면 정상으로 간주되는데 우리나라 성인 남녀의 혈청 α-토코페롤 농도는 0.68-1.20 mg/dL로 [37-41] 정상범위에 속하고 결핍수준은 거의 없는 것 으로 보고되었다.
부족 시 나타나는 주요 건강문제로는 근육과 신경의 공조가 제대로 일어나지 않아 발생하는 운동실조 (ataxia), 골격근증(skeletal myopathy), 색소침착 망막증(pigmented retinopathy) 등을 들 수 있다. 이러 한 비타민 E 부족 증세와 함께 혈청 내 비타민 E 농도가 매우 낮을 경우(2.3 μmol/L 혹은 1.0 μmol/L 미만) 비타민 E의 결핍으로 판정할 수 있다. 비타민 E 결핍 및 그에 따른 질환의 주요 원인은 식사 부족보 다는 지단백질대사이상(abetalipoproteinemia) 이나 α-토코페롤 수송 단백질 유전자에 결함 때문으로 알 려져 있다 [42-44]. 비타민 E 결핍이 의심되는 사람의 평가에 과산화수소나 다른 산화제를 이용한 용혈현 상을 이용하였는데 [33, 45], 혈액의 α-토코페롤 농도가 14 μmol/L(600 μg/dL) 이상이면 용혈현상이 방지 되는 것으로 보고되었다 [33].
2-2. 결핍 예방을 위한 섭취기준 및 한국인 섭취실태
2-2-1. 한국인의 비타민 E 섭취기준 및 섭취실태
한국인의 비타민 E 섭취기준을 설정함에 있어서 비타민 E 섭취량에 따른 혈액의 토코페롤의 농도에 대 하여 한국인을 대상으로 단계적으로 조사한 연구가 없고, 과산화수소에 의한 적혈구 용혈정도를 측정한 연구도 없어 한국인의 평균필요량 결정에 어려움이 있다. 또한 한국인을 대상으로 비타민 E 복합체의 개별 적 섭취량을 체계적으로 연구한 자료가 매우 부족한 실정이다.
한국인이 식품을 통해 섭취하는 비타민 E의 주요 형태는 α-토코페롤과 γ-토코페롤이고 상당한 양의 γ- 토코페롤이 한국인의 혈액 및 체조직에 존재함을 고려할 때 α-토코페롤만을 활성 비타민 E로 인정하는 관 점은 수용하기 어려운 현실이다. 이와 같은 관점은 미국과 일본을 제외하고 호주, 뉴질랜드 및 유럽과 동 일한 견해이다. 그런데 한국에서 보고되는 비타민 E 섭취 관련 연구는 대부분 비타민 E의 단위로 α-토코 페롤 당량(mg α-TE)이 아닌 4종의 토코페롤과 4종의 토코트리에놀 함량의 단순 합으로 계산한 비타민 E 의 mg으로 보고되는 경우가 대부분으로 우리 국민의 섭취량을 비타민 E 섭취기준과 비교하여 평가하기에 어려움이 있다 하겠다.
따라서 우리 국민의 상용식품에 포함되어 있는 비타민 E의 함량에 대한 완성도 있는 데이터베이스의 절대적인 부족, 그리고 4종의 토코페롤과 4종의 토코트리에놀 섭취에 따른 혈액의 농도 변화에 대한 연구의 부재는 앞으로 보다 실질적인 한국인 영양소 섭취기준 개정을 위하여 극복해야 할 과제라고 할 수 있다.
2-2-2. 한국인의 비타민 E 섭취 기준 제정시의 고려사항
(1) 권장섭취량이 아닌 충분섭취량
비타민 E의 권장량은 아직 한국인을 대상으로 한 관련 자료가 충분하지 않아 권장섭취량이 아닌 충분섭 취량으로 제정되었다. 이는 한국인 각 연령층의 비타민 E 섭취량의 중앙값을 기준으로 한 것으로 거의 모 든(97-98%) 건강한 인구집단의 영양소 필요량을 충족시키는 섭취량 추정치인 권장섭취량이 아님을 고려하 여야 한다.
(2) 모든 형태의 비타민 E를 권장량에 포함
미국, 일본 등에서는 자연에 존재하는 비타민 E 중 β-,γ-,δ-토코페롤은 α-토코페롤로 전환될 수 없고, α-토코페롤 수송 단백질에 의해 잘 인식되지 못하므로, α-토코페롤 만을 권장량에 포함시켰다. 그런데 한 국인의 많은 γ-토코페롤 섭취 및 그 항산화 기능을 경시할 수 없어 2020년 한국인 비타민 E 충분섭취량에 는 2015년도와 동일하게 모든 형태의 비타민 E를 포함시켰다. 따라서 동일한 양의 비타민 E를 섭취할 경 우 한국인의 비타민 E 섭취량은 미국이나 일본에서 보고되는 섭취량보다 많은 것으로 나타나게 됨을 고려해야 한다.
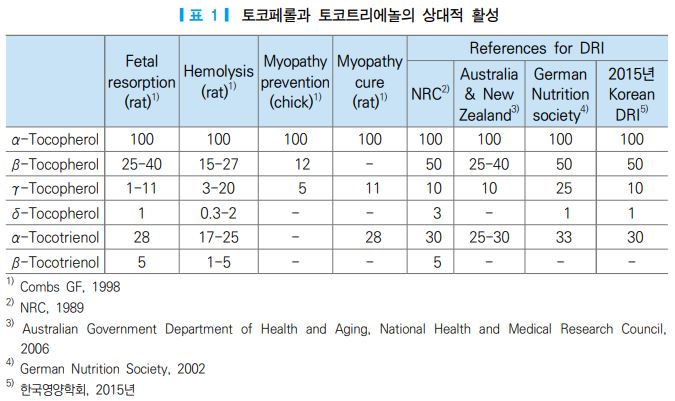
비타민 E의 8가지 화합물(각각 4가지의 토코페롤 및 토코트리에놀)에 대한 동물실험 결과를 바탕으로 생리적 활성을 비교한 후, α-토코페롤 당량(α- tocopherol equivalent, α-TE)이 설정되었다.
태아재흡수(fetal resorption), 용혈(hemolysis), 근육병증 예방(myopathy prevention) 및 근육병증 치료(myopathy cure) 등 4종의 지표 [46, 47]와 1989년도 미국 국립 연구회의 [47] 및 호주/뉴질랜드 [48], 독일/스위스 [49]와 한국영양학회 [50]에서 영양소 섭취기준 제정에 토코페롤과 토코트리에놀의 상대적 활 성이 아래 표에 제시되어 있다. 현재 미국과 일본은 α-토코페롤만을 비타민 E로 인정하고 있으나, 호주, 뉴질랜드 및 유럽국가에서는 8종의 비타민 E 화합물을 모두 비타민 E로 인정하고 있다. 항산화성, 항감염 성 등 생화학적 기능 측면을 이용한 비타민 E의 생리적 활성 지표는 아직 개발되어 있지 않다.
(3) 남성과 여성의 충분섭취량 동일
한국인 남성의 비타민 E 섭취량은 여성보다 많은 것으로 조사되었으나 여성의 체지방이 남성보다 많은 것을 고려하여 남성과 여성의 충분섭취량을 동일하게 제정하였다. 체지방이 많은 여성의 경우 또는 비만인 사람의 경우 충분섭취량보다 더 많은 비타민 E가 요구될 수 있다 [51, 52].
2-2-3. 외국인의 비타민 E 섭취기준 및 섭취실태
미국/캐나다에서는 비타민 E 영양소 섭취기준 [2]을 제정할 때 체내에서의 수송 및 대사의 특성을 고려 하여 비타민 E의 활성을 갖는 형태로 2R-입체이성체(2R-stereoisomer)의 α-토코페롤만을 활성 비타민 E로 인정하여 권장량을 설정하였으며, 일본과 필리핀에서도 이러한 미국의 관점을 수용하고 있다. 미국에서는 성인의 비타민 E 1일 권장섭취량을 15 mg으로 제정하였는데 이는 Horwitt의 연구 [32, 34]를 근거로 12 mg을 평균필요량으로 수용하고 20%의 표준변이를 가산한 결과이다. 미국의 국민건강영양조사(NHANESIII) 자료에 따르면 31-50세 남자의 경우 1일 총 비타민 E 섭취량이 12.9 mg(10.3 mg α-토코페롤), 동일연 령층 남자의 경우 1일 총 비타민 E 섭취량이 9.1 mg(7.3 mg α-토코페롤)으로 나타났다 [2]. 또한 미국의 학교급식 프로그램 분석결과 학교급식에서 비타민 E가 부족한 것으로 나타났으며, 비타민 E 섭취상태가 미국의 영양소 섭취기준에 못 미치는 학생이 6-8세는 64%, 9-13세는 87-91%, 14-18세는 95-97%로 비타민 E 섭취 부족한 학생의 비율이 높은 것으로 조사되었다 [2]. 이와 같은 결과는 설문지 답변자가 섭취량을 실제보다 적게 보고하거나 또는 식품준비 중에 첨가된 지방과 기름을 간과하거나 잘 모르는 경우에 기인한 것으로 보고되었다.
일본은 미국과 동일하게 α-토코페롤만을 활성 비타민 E로 인정하여 성인 남성 6.5mg α-토코페롤, 여성 6.5 mg α-토코페롤을 1일 충분섭취량으로 제정하고 있다 [53]. 일본인 성인을 대상으로 섭취량과 혈중 α- 토코페롤 농도를 측정한 보고에 따르면 [54-56] 이들 연구 집단의 1일 α-토코페롤 평균 섭취량은 5.6-11.1 mg이었으며, 연구된 모든 집단에서 혈중 농도 평균값이 22 μmol/L 이상으로 유지되고 있었다.
2-2-4. 생애주기별 한국인 비타민 E 섭취기준
(1) 영아기(1세 미만)
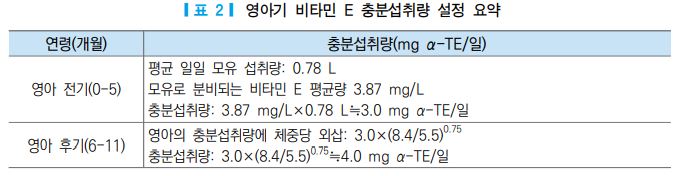
영아의 식이 섭취량에 따른 비타민 E의 체내 상태 변화에 대한 기능적 지표가 없으므로 영아의 비타민 E 권장량은 전적으로 모유 수유를 하는 영아의 평균 비타민 E 섭취량을 충분섭취량으로 정하였다. 모유의 비타민 E 농도가 387 μg/100 mL이므로 [57-59], 영아 전기(0-5개월)의 비타민 E 충분섭취량은 하루 3.0 mg α-TE(3.87 mg/L×0.78 L=3.0 mg α-TE)으로 제정되었다. 영아 후기(6-11개월)의 충분섭취량은 0-5개 월 영아의 섭취량에서 대상체중으로 외삽하여 2015년도 권장기준과 동일한 하루에 4.0 mg α-TE [3.0×(8.4/5.5)0.75=4.1→ 4.0 mg α-TE]로 정하였다.
(2) 성장기(1-18세)
2015년도 유아, 아동, 청소년들의 섭취기준은 2008-2012년 국민건강영양조사의 식품섭취량 자료 [60]와 2012년 한국영양학회 영양소 데이터베이스 [61]를 기반으로 성인의 충분섭취량으로부터 체중과 성장률을 고려하여 제정하였다. 2020년도 비타민 E 충분섭취량은 2015년 충분섭취량과 동일하게 설정되었다. 그런 데, 한국인의 식품섭취기준을 설정하는데 있어서 기본자료가 되는 우리나라의 식품성분표 및 섭취량의 대 부분이 비타민 E 섭취기준의 단위인 mg α-TE로 표현되지 않고, 4종의 토코페롤과 4종의 토코트리에놀 함량의 단순 합인 mg [62]으로 계산되어 비타민 E 섭취량을 과대평가 하는 제한점의 극복이 시급하다.
① 유아(1-5세)
2008-2012년 국민건강영양조사 식품섭취량 자료 [61]와 한국영양학회 영양소 데이터베이스 [62]를 이용 하여 분석한 결과에 따르면 1-2세에는 비타민 E 섭취 중앙값이 4.8 mg α-TE, 3-5세에는 6.2 mg α-TE이 었다. 그런데 성인의 필요량으로부터 추산한 필요량은 1-2세에는 4.48 mg, 3-5세에는 5.38 mg으로 나타나 1-2세에는 영아보다 1 mg 추가된 5 mg α-TE, 그리고 3-5세에는 1-2세보다 1 mg 추가하여 6 mg α-TE로 정하였다.
② 아동(6-11세)
2008-2012년 국민건강영양조사 식품섭취량 자료 [60]와 한국영양학회 영양소 데이터베이스 [61]를 이용 하여 분석한 결과에 따르면 남아의 비타민 E 섭취 중앙값이 6-8세에서 9.0 mg α-TE, 9-11세 10.3 mg α
-TE이고 여아의 경우 6-8세 7.5 mg α-TE, 9-11세 8 mg α-TE으로 남아의 섭취량이 여아보다 높은 것으로 나타났다. 그러나 여아와 남아의 체지방 비율 및 성인의 필요량으로부터 추산한 값 등을 고려하여 6-8세 7 mg α-TE, 9-11세 9 mg α-TE로 정하였다.
③ 청소년(12-18세)
2008-2012년 국민건강영양조사 식품섭취량 자료 [60]와 한국영양학회 영양소 데이터베이스 [61]를 이용 하여 분석한 결과에 따르면 12-14세 청소년의 경우 남아의 비타민 E 섭취 중앙값이 10.8 mg α-TE이고 여아의 경우 9.5 mg α-TE 이었다. 그런데 성인의 충분섭취량으로부터 추산한 충분섭취량은 남아 11.29 mg α-TE 여아 12.44 mg α-TE 로 성인의 충분섭취량과 유사하였다. 따라서 12-14세 청소년의 충분섭취량 은 2015년에 비하여 1mg α-TE 상향 조정하여 11 mg α-TE 로 정하였다. 15-18세 청소년의 경우 2008-2012년 국민건강영양조사 식품섭취량 자료 [60]와 한국영양학회 영양소 데이터베이스 분석 결과 [61] 남아의 중앙값은 13 mg, 여아의 중앙값은 9.6 mg으로 나타났으며, 성인의 충분섭취량으로부터 추산한 값 은 남아 13.13 mg α-TE, 여아 11.66 mg α-TE 이었다. 따라서 청소년기 불규칙한 영양소 섭취 등을 고려 하여 15-18세의 청소년의 충분섭취량은 2015년에 비하여 1 mg α-TE 상향 조정하여 성인과 동일한 12 mg α-TE로 정하였다.

(3) 성인기(19-64세)
2008-2012 국민건강영양조사 식품섭취량 자료 [60]와 한국영양학회 데이터베이스 [61]를 이용한 분석결 과에 따르면 성인 19-49세 남자의 비타민 E 섭취 중앙값은 13.6 mg α-TE, 여자는 9.4 mg α-TE이었고, 50-64세 남자의 비타민 E 섭취 중앙값은 9.2 mg α-TE, 여자는 6.7 mg α-TE 이었다. 2007-2008년 국민건 강영양조사 자료를 바탕으로 조사한 우리나라 성인들의 비타민 E섭취 중앙값은 20-49세 남자는 12.7 mg α-TE, 여자는 8.6-9.8 mg α-TE, 50-64세 남자는 9.2 mg α-TE, 여자는 6.7 mg α-TE이었다 [63]. 2015년 우리나라의 비타민 E 충분섭취량 기준은 섭취량 조사 결과인 성인들의 비타민 E 섭취량 및 남녀의 지방함 량 등을 고려하여 남자와 여자 동일하게 12 mg α-TE로 정하게 되었다.
그런데 2013-2015년 국민건강영양조사 대상자의 24시간 회상법 자료를 바탕으로 조사한 우리나라 성인 들의 평균 비타민 E 섭취량은 남성 7.5 mg α-TE, 여성 6.4 mg α-TE로 보고되었으며, α-, β-, γ-, δ-토코 페롤의 기여율은 α-토코페롤(남성: 6.5 mg/d, 여성: 5.7 mg/d), γ-토코페롤(남성: 6.0 mg/d, 여성: 4.8mg/d), δ-토코페롤(남성: 3.9 mg/d, 여성: 2.8 mg/d), β-토코페롤(남성: 0.5 mg/d, 여성: 0.4 mg/d)로 나타났다 [64]. 한편, 2007-2009년도 국민건강영양조사 대상자의 비타민 E 섭취량을 4종의 토코페롤의 단 순 합으로 계산할 경우 비타민 E 섭취량은 남성 19-29세 15.8 mg/d, 30-49세 17.0 mg/d, 50-64세 15.3 mg/d, 여성 19-29세 13.0 mg/d, 30-49세 12.6 mg/d, 50-64세 11.8 mg/d으로 추정되었다 [64].
이와 같이 섭취량 평가에 사용되는 단위의 혼재 및 데이터베이스의 완성도의 문제점 등으로 정확한 비 타민 E의 섭취량을 평가하는 데는 제한점이 있다고 하겠다. 또한 α-토코페롤 만을 활성 비타민 E로 간주 하는 미국이나 일본과 다르게 우리나라는 아직도 4종의 토코페롤과 4종의 토코트리에놀을 모두 활성 비타 민 E로 간주하므로 비타민 E에 대한 데이터의 차이로 인한 국가간 비교가 매우 어려운 실정임을 간과해서 는 안된다.
뿐만 아니라 미국의 식품의약국에서는 2016년에 자연형 α-토코페롤인 RRR-α-토코페롤과 합성형 α-토 코페롤인 all-racemic-α-토코페롤의 생체역가(biopotency) 비율을 1.36:1에서 2:1로 변경하여 보충제 라벨 에 표시하기로 결정하였다 [8]. 이와 같은 급격한 생체역가 비율의 변경은 기존의 1.36:1은 동물실험을 통 한 태아흡수(fetal resorption) 실험결과 [65] 및 α-토코페롤 수송단백질(TTP)에 대한 α-토코페롤 입체이성 질체의 상대적인 친화력을 외삽하여 결정하였으나, 중수소화 토코페롤(deuterated tocopherol)을 이용한 연구에서 RRR-α-토코페롤과 합성형 α-토코페롤인 all-rac-α-토코페롤의 생체역가(biopotency) 비율을 2:1 하는 것이 타당하다는 연구가 지속적으로 보고되었기 때문이다 [7, 66]. RRR-α-토코페롤과 all-rac-α-토코 페롤의 서로 다른 건강 효과 및 생리적 활성이 지속적으로 논의되고 있으며 [65, 67] 우리나라도 앞으로 이에 대한 적극적인 논의가 필요하다고 할 수 있다.
2020 한국인 영양소 섭취기준은 2015년과 동일하게 우리나라 비타민 E 섭취량 조사결과를 반영하고, 체중은 남자가 여자보다 높으나 체지방은 여자가 남자보다 많은 점 및 남・여의 충분섭취량을 다르게 설정 할 과학적 근거가 부족한 점을 고려하여 성별에 관계없이 동일하게 12 mg α-TE로 설정되었다.

(4) 노인기(65세 이상)
65세 이상에서도 비타민 E 충분섭취량을 성인과 같은 기준인 12 mg α-TE로 정하였다. 그 이유는 노인 층의 비타민 E 섭취 부족이 식사량 및 지방 섭취 부족에서 기인한 것으로 생각되고 별도의 영양제 섭취는 포함이 되지 않았을 것으로 추정되기 때문이다. 또한 비타민 E의 노화방지 기능 등을 고려할 때 노인기의 비타민 E 섭취량을 성인기와 다르게 설정할 과학적 근거가 부족하다. 이와 같은 수준은 독일, 스위스의 기준과 비슷하나 이들 나라에서는 65세가 넘는 노인층에서 성인보다 1 mg 씩 낮추었다. 2015년 일본의 70세 이상의 노인층 비타민 E 섭취기준은 19-50세 성인의 충분섭취량과 동일하게 유지하고 있다. 그러나 2008-2012년 국민건강영양조사 식품섭취량 자료 [60]와 한국영양학회 영양소 데이터베이스 [61]를 활용하 여 분석한 자료에 나타난 노인층의 비타민 E 섭취의 중앙값이 65-74세에서는 남자가 7.9 mg α-TE, 여자5.9 mg α-TE, 75세 이상에서는 남자 5.3 mg α-TE, 여자 4.1 mg α-TE로 매우 낮기 때문에 지속적으로 추가적인 자료의 축적 및 계속적인 논의가 필요하다.

(5) 임신기
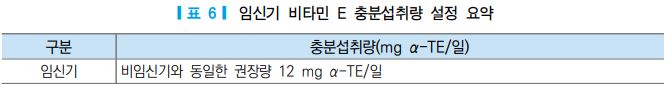
임신기의 비타민 E의 충분섭취량은 비임신 여성과 동일하게 설정하였는데 그 근거는 다음과 같다. 임신 기간 동안에 혈중 지질 농도 증가로 α-토코페롤의 농도가 상승하지만 [68] 태반을 통한 비타민 E의 이동은 큰 변화가 없는 것으로 보고되었다 [69]. 또한 미숙아의 경우 비타민 E 결핍으로 인한 용혈성 빈혈이 발생 할 수 있다고 보고되었으나 [70], 임신 중 비타민 E 섭취 증가와 미숙아의 관련성은 보고된 바 없다. 뿐 만 아니라 한국인 임신부의 비타민 E 섭취량은 12-16 mg α-TE으로 성인여성의 충분섭취량을 상회하며 [71], 그에 따른 문제는 보고된 바 없다. 따라서 임신부에 대한 비타민 E 충분섭취량의 부가량은 설정하지 않았다.
(6) 수유기
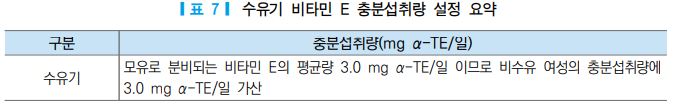
수유기에는 유즙으로 분비되는 비타민 E 양이 약 300-540 μg/100 mL [57-59]이며, 영아의 하루 모유 섭취량을 약 0.78 L 임을 고려할 때 모유로 분비되는 비타민 E의 양은 2.3-4.0 mg/일로 평균 약 3.0 mg α-TE/일이 되므로 수유부의 1일 비타민 E 충분섭취량은 비수유 여성의 충분섭취량에 3.0 mg α-TE을 가 산하였다.
2-3. 만성질환 위험감소를 위한 섭취기준
2-3-1. 비타민 E 섭취와 만성질환의 연관성
(1) 심순환계질환
동맥경화증과 같은 심순환계질환의 발생은 저밀도지단백질(LDL)의 산화와 밀접하게 연관되어 있다 [72, 73]. 따라서 산화를 방지할 수 있는 비타민 E는 심순환계질환의 예방 및 치료에 사용되어 왔다. 대규모의 역학 연구에서는 비타민 E 섭취가 관상동맥 심장질환의 위험도를 낮출 수 있음이 반복적으로 보고되었으 며 [74, 75], 유럽 16개국을 대상으로 한 역학 연구에서도 혈액의 α-토코페롤 농도가 허혈성심장질환에 의 한 사망률과 역의 상관관계가 있다고 보고되었다 [76]. 또한 동물모델을 이용한 연구에서 동맥경화가 쉽게 유발되고 비타민 E 또한 결핍되는 두개의 녹아웃(double knockout) 마이스에게서 동맥경화만 쉽게 유발 되는 하나의 녹아웃(single knockout) 마이스에 비하여 유의적으로 커다란 대동맥 병변 및 근위 대동맥의 지질 과산화가 증가하였음을 보여줌으로써 비타민 E가 산화적 손상에 의한 동맥경화 병변을 방어할 수 있 음을 증명하였다 [77].
그러나 임상연구에서는 심혈관계질환에 대한 α-토코페롤의 효과가 상충되는 결과를 보인다. 비타민 E 보충제 섭취가 내피기능 및 심순환계질환 위험도의 마커가 되는 내피세포의존성 혈관확장에 영향을 준다고 보고한 메타연구 [78]가 있는 반면, 13개의 무작위 임상시험을 분석한 또다른 메타연구에서는 비타민 E 보충제 섭취가 뇌졸증을 예방하는데 도움이 되지 않는다고 보고하였다 [79]. 또한 단기간의 토코트리에 놀을 이용한 무작위 임상시험에서는 토코트리에놀을 섭취한 연구대상자의 혈액 토코트리에놀 농도는 증가 하였으나 혈관기능에는 변화가 없는 것으로 보고되었다 [80]. 이와 같은 상이한 연구결과는 비타민 E의 종 류 및 형태 그리고 연구대상자 등에 따라 상이한 연구결과를 얻게 되는 비타민 E 임상연구의 어려움을 반영한다고 할 수 있다.
(2) 암
산화적 스트레스는 세포 성분을 손상시키고 암의 발병과 연관되어 있다고 할 수 있고, 자유 라디칼을 제거할 수 있는 기능이 있는 α-토코페롤은 DNA 손상을 방어하고 암 발병을 예방 할 수 있다고 할 수 있다 [81]. 그러나 α-토코페롤 보충제 섭취가 항산화작용에 의한 DNA 손상을 억제한다는 증거가 부족하여 [82-84] 비타민 E의 항산화작용이 암을 예방하는 기전인지에 대해서는 명확하지 않다. 전임상 연구에서는 α-토코페롤과 그 유도체가 대장의 종양형성에 효과적이지 못한 것으로 나타났으나, γ-토코페롤과 α-토코 페롤 복합체는 대장암, 폐암, 전립선암, 유선암 등에서 효과가 있음이 보고되었다 [85]. 또한 토코트리에놀 은 화학요법, 약물 또는 폴리페놀과 같은 식이성분과의 상호작용을 통하여 항암효과가 있는 것으로 보고된 바 있다 [86]. 비타민 E 섭취가 췌장암 [87], 대장암 [88], 방광암에 의한 사망 [89]의 위험율을 낮추는 것으 로 보고되었으며, 혈액 α-토코페롤 농도는 전립선암 위험율과 역의 상관관계가 있음이 보고되었다 [90]. 반면에 비타민 E 보충제 섭취는 대장암 [91], 대장암에 의한 사망(92), 위암에 의한 사망 [93]의 위험율과 관련이 없는 것으로 나타났다. 따라서 비타민 E의 보충제 섭취에 의한 암의 예방에 대한 과학적 근거는 아직까지 충분하지 못하다 할 수 있다.
(3) 면역계 질환
비타민 E와 면역계의 연관성은 알레르기성 기도질환과 폐기능을 중심으로 연구되었다. 혈액 α-토코페 롤 농도는 폐활량 마커와 양의 상관관계가 있음이 보고되었고 [94] α-토코페롤이 노화에 따른 T-Cell의 기 능적 퇴화를 억제 할 수 있다고 보고되었다 [95]. 항산화 영양소의 섭취는 천식 유병율과 역의 상관관계가 있음이 보고되었고 [96], 내피세포에서 α-토코페롤이 단백질 키나제(protein kinase) C를 억제하여 백혈구 모집(recruitment of leukocytes)을 억제함으로써 염증성 면역반응을 조정한다고 보고 된 바 있다 [97, 98]. α-토코페롤은 동물모델을 이용하여 심장에서 면역과 관련된 유전자의 발현을 조절하는 것이 보고되 었으며 [99], 감염과 관련되는 다양한 유전자를 조정하는 것으로 보고되었다 [100]. 이와 같은 α-토코페롤 에 의한 유전자 발현은 자연형 RRR α-토코페롤이 합성형 all-rac α-토코페롤보다 월등히 탁월한 것으로 보고되었다 [101]. 한편 γ-토코페롤은 호중구 기도 염증(neutrophilic airway inflammation) [102] 및 천식 의 염증을 완화시키는데 [103] 도움이 있는 것으로 보고된 바 있다. 즉 인체내 면역반응은 비타민 E의 종류 및 형태에 따라 세포내 타겟에 다르게 반응하고, 생체 역가도 다르다고 할 수 있다.
(4) 중추신경계질환
동물실험에서 α-토코페롤은 세포성분의 산화적스트레스를 억제함으로써 신경변성을 억제하고 뇌건강에 도움이 되는 것으로 보고되었다 [104, 105]. α-토코페롤 전이단백질(α-TTP) 녹아웃(knockout)으로 심각한 α-토코페롤 결핍을 일으킨 일련의 동물실험에서 나이가 들어 감에 따라 소뇌 [106], 척수 [107]에 구조적 이상을 나타내며, 행동에 문제를 야기함 [107]이 보고되었다. 이와 같은 결과는 비타민 E 결핍으로 사람에 게 나타날 수 있는 운동실조증을 설명하는데 도움이 된다. 운동실조증이 있는 사람의 경우 α-토코페롤 전 이단백질(α-TTP) 유전자의 소실 또는 변이에 의하여 심각한 신경기능장애를 나타낸다 [108]. 비타민 E 결 핍에 의한 운동실조증 환자의 경우 지속적인 α-토코페롤 보충에 의해 혈액의 α-토코페롤 농도를 정상화함 으로써 부분적으로 신경장애를 복구 할 수 있음이 보고되었다 [109]. 또다른 신경계질환인 알츠하이머병 및 치매와 α-토코페롤과의 관련성은 상이한 결과가 보고되었다. 역학연구에서는 토코페롤 섭취가 많을수 록 알츠하이머병의 위험율이 낮은 것으로 보고되었고 [110], 알츠하이머병이 있는 사람들은 혈액 α-토코페롤 농도가 낮은 경향이 있는 것으로 보고되었다 [111]. 반면에 뇌의 α-토코페롤 농도는 알츠하이머병과 관련 성이 없었고 [104], 혈액의 α-토코페롤 농도가 인지기능과 관련성이 없는 것으로 보고되기도 하였다 [112]. 이와 같은 상이한 연구 결과를 고려할 때 알츠하이머병과 관련하여 토코페롤, 토코트리에놀과 같은 다양한 비타민 E의 상호작용을 간과해서는 안된다는 제안도 있으며 [113], α-토코페롤의 항산화기능과 신경계 질 환과의 관련성 [114] 뿐만 아니라, α-토코페롤의 항산화기능 이외의 기능으로서의 신경계 건강에 대한 기 여도 보고되고 있다 [115].
2-3-2. 만성질환 위험감소를 위한 섭취기준 설정
비타민 E는 항산화기능으로 인하여 다양한 만성질환과 연관성이 있는 것으로 보고되었으며, 특히 비타 민 E와 심혈관계질환, 암, 면역계질환, 그리고 신경계질환과의 연관성은 보다 잘 정립되어 있다고 할 수 있다. 그 외 당뇨병 [116-118], 황반변성 [119, 120] 백내장 [121, 122] 과의 연관성도 지속적으로 보고되 었다. 그럼에도 불구하고 아래와 같은 이유에 의해서 비타민 E의 만성질환 위험감소를 위한 섭취기준 설정 은 유보하였다.
● 비타민 E의 섭취 부족 시 나타나는 운동실조와 같은 체내 증상은 사람에게서 거의 발견되지 않으며, 고용량 섭취에 따른 큰 유해영향도 보고된 것이 미비함
● 미국과 일본에서는 권장량 설정을 위한 활성 비타민 E로 α-토코페롤 만을 이용하며 이는 간에서 α-토코페롤 만이 α-토코페롤 수송단백질(α-TTP)에 의해 신체조직으로 운반되고, 그 외 β-, γ-, δ- 토코페롤(tocopherol)과 α-, β-, γ-, δ- 토코트리에놀(tocotrienol)은 α-토코페롤 수송단백질과의 친 화력이 미비하기 때문임. 그런데 우리나라에서는 α- β-, γ-, δ- 토코페롤(tocopherol)과 α-, β-, γ-, δ- 토코트리에놀(tocotrienol)을 모두 활성 비타민 E로 이용하고 있어 실질적인 활성 비타민 E의 목표 량 선정에 혼선이 올 수 있음
● 현재 우리나라에서는 식품의 비타민 E 함량을 α- β-, γ-, δ- 토코페롤(tocopherol)과 α-, β-, γ-, δ- 토코트리에놀(tocotrienol)의 총합인 mg으로 제시하고 있어 권장량에서 제시하고 있는 mg α-TE와는 커다란 차이가 있을 수 있음
● 자연형 RRR α-토코페롤과 합성형 all-rac α-토코페롤의 생체 역가(biopotency) 비율이 미국 에서는 2016년부터 1.36:1에서 2:1로 변경되었음. 그 이유는 기존 동물모델을 이용한 태아흡수(fetal resorption) 연구를 통한 1.36:1이 중수소화 토코페롤을 이용한 보다 완성도 있는 연구들에서 2:1의 비율이 적합함이 밝혀졌기 때문임. 그럼에도 불구하고 우리나라는 기존의 비율인 1.36:1을 유지하고 있어 α-토코페롤 입체 이성체의 생체 역가에 대한 논의가 선행되어야 함
3 안전확보를 위한 섭취기준
3-1. 안전을 위한 섭취기준 설정 시 고려사항
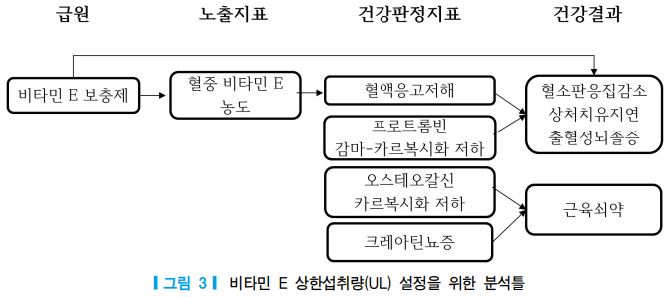
일반적으로 식품을 통한 비타민 E의 섭취는 건강에 도움이 되는 것으로 알려져 있으나 [123, 124], 보충 제 등의 형태로 α-토코페롤을 과잉 섭취할 때 건강에 유해할 수 있음이 보고되었다. 비타민 E 과잉섭취 시 나타나는 증상으로는 크레아틴뇨증, 혈소판 응집 감소, 상처 치유 지연, 무월경증, 피로, 복시, 근육쇠약 등을 들 수 있다 [125-127].
비타민 E 과잉섭취의 독성종말점으로 그동안 보고되었던 다양한 유해현상 중 출혈독성에 관한 지표가 주로 적용되고 있으며 관련된 지표로는 혈액응고 저해, 프로트롬빈 감마-카르복시화 저하, 오스테오칼신의 카르복시화 저하 등과 같은 비타민 K 길항작용 등을 들 수 있다. 미국의학협회 [2] 는 비타민 E에 대한 상한섭취량을 1,000 mg/일로 설정하였는데, 이는 흰쥐를 대상으로 한 용량-반응 평가 [128]에 의해 출혈독 성을 일으키지 않는 최저유해용량이 RRR-α-tocopheryl acetate 형태로 500 mg/kg BW/일이었으며, 불확 실계수 36, 성인 남녀의 표준체중에 대한 평균값을 적용한 결과이다. 여기에서 불확실계수 36은 최저유해 용량의 최대무해용량으로의 전환, 아만성섭취량의 만성섭취량으로의 환산, 동물실험 결과를 사람에게 적 용, 민감도에 대한 개인 간 변이 고려 등 다양한 변수들을 모두 고려하였다. 비타민이 독성종말점을 출혈 독성에 두고 최저유해용량을 500 mg/kg BW/일로 정한 것은 Takahashi 등 [129]과 Abdo 등 [130]의 동물 모델을 이용한 실험을 통해서도 타당한 것으로 확인되었다. 영국의 비타민・미네랄 전문가 위원회 [131]과 유럽연합 식품과학위원회 [132]은 Meydani 등 [133]과 Stephens 등 [134]의 용량-반응 평가를 활용하여 800 IU의 all-rac-α-토코페롤(540 mg α-토코페롤에 해당)을 각각 4개월과 510일 복용시켜 유해현상이 나 타나지 않은 연구결과를 근거로 540 mg α-토코페롤을 최대무해용량으로 정하였다. 그러나 영국과 유럽연 합은 동일한 최대무해용량을 적용하였음에도 불구하고, 서로 다른 불확실계수(영국 1, 유럽연합 2)를 적용 함으로써, 비타민 E에 대한 상한섭취량이 영국은 540 mg/일, 유럽연합은 300 mg/일로 설정하였다. 일본 은 건강한 성인 남자를 대상으로 한 Morinobu 등 [135]의 독성종말점 연구에서 800 mg α-토코페롤/일을 28일간 투여한 실험군(n=14)과 대조군(n=8)간에 출혈독성(혈소판 응집, 혈액응고)이 유의적인 차이가 나 타나지 않음을 고려하여, 2010 일본인의 식사지침기준에서 성인 남자 18-29세 군에 대한 비타민 E 상한섭 취량을 800 mg/일로 설정하였고, 2015년 개정된 식사지침기준에서도 이 기준을 그대로 유지하였다.
한편 Hathcock 등 [136]은 임상자료를 고찰한 결과, 성인에게 비타민 E를 1,073 mg α-TE/일까지 투여 시 안전하다고 보고하였으나, 이 연구 결과는 용량-반응 평가를 적용해 얻어진 결과가 아니어서 상한섭취 량 설정에 적용하기는 어렵다. 그리고 Miller 등 [137]은 메타분석을 통해 비타민 E 보충제를 400 IU/일 (270 mg/일)이상 섭취한 대상자들의 사망률이 400 IU/일 미만 투여한 대상자들보다 유의하게 증가함을 보고하였으며, 이를 근거로 400 IU/일 이상의 비타민 E 섭취는 건강에 위험을 초래할 수 있으므로 400 IU 이상의 비타민 E 과잉섭취의 위험성을 경고하였다.
3-2. 안전 확보를 위한 섭취기준 및 한국인 섭취실태
비타민 E는 식품으로 섭취할 때 일반적으로 고용량 섭취에도 큰 유해영향이 없는 것으로 알려져 있다. 따라서 심혈관계질환 예방을 위한 목적으로 400-600 IU의 비타민 E 보충제를 투여한 대규모 중재연구가 이루어졌으며 그 결과 심혈관계질환이 감소되었기 때문에 많은 사람들이 비타민 E 보충제를 복용하게 되 었다. 그러나 비타민 E를 800-1,200 mg α-TE이상 섭취할 경우에 부작용이 발생할 수 있다고 보고되었다. 위장질환이 생기거나 혈장 티록신 수준이 감소될 수 있으며 비타민 K의 흡수를 방해하여 혈액응고에 문제 를 초래할 수 있다 [138]. 뿐만 아니라 아스피린 상용과 비타민 E 과잉 섭취에 의한 출혈의 위험성이 증가 할 수 있음이 지적되기도 하였다 [139]. 또한 과량의 비타민 E 섭취가 약물대사에 영향을 미칠 수 있는 것으로 알려졌다. 과량의 비타민 E는 체내에서 CYP3A4를 통해 약물대사를 촉진시킬 수 있는 가능성이 있으며, 혈청지질 강하제인 심바스타틴(simvastatin) [140]이나 에스트로겐(estrogen) [141]의 대사가 촉진되어 약효를 감소시킬 수 있다고 보고 되었다. 뿐 만 아니라 대규모 메타분석 연구는 비타민 E 보충제 섭 취를 통하여 도달할 수 있는 1,000 IU 이상의 비타민 E 섭취가 전반적인 사망률을 높인다는 결과를 보고함 으로써 무분별한 비타민 E 보충제 섭취의 위험성이 지적되기도 하였다 [142]. 그러나 비교적 최근에 보고 된 30년에 걸친 전향적(Prospective) 코호트 연구에서 ATBC연구(Alpha-Tocopherol, Beta-Carotene Cancer Prevention) 참여 대상자에게서 baseline α-토코페롤 농도가 높을 경우 전반적인 사망 위험율이 감소한 결과를 보고 함으로써 식품을 통한 비타민 E의 섭취가 건강유지에 효과적임을 다시 한번 증명하였다 [123, 124].
2008-2012년 국민건강영양조사 식품섭취량 자료를 [60] 2015년 한국영양학회 영양소 데이터베이스를 이용하여 분석한 결과에 의하면 1세 이상 전체 연령군의 1일 식품을 통한 비타민 E 섭취량에 대한 중간값 은 10.1 mg/일, 평균 97.5 백분위수는 40.9 mg/일, 상한섭취량 초과 평균 비율은 0%인 것으로 나타났다. 따라서 대부분의 한국인은 비타민 E를 과잉섭취 하지 않는 것으로 볼 수 있다. 그러나 우리나라 중년기를 대상으로 비타민・무기질 보충제를 통한 비타민 E 섭취량을 조사한 연구에서, 비타민 E 보충제 복용군 중 21%가 비타민 E 상한섭취량(540 mg/일)보다 높은 600 mg/일을 섭취하는 것으로 보고되어, 보충제를 통 한 비타민 E의 과잉섭취를 주의할 필요가 있음이 지적되었다 [143].
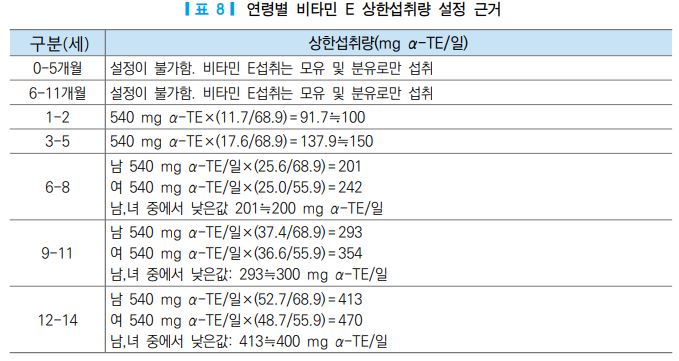
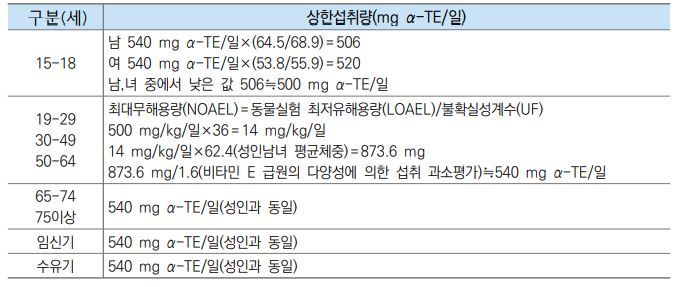
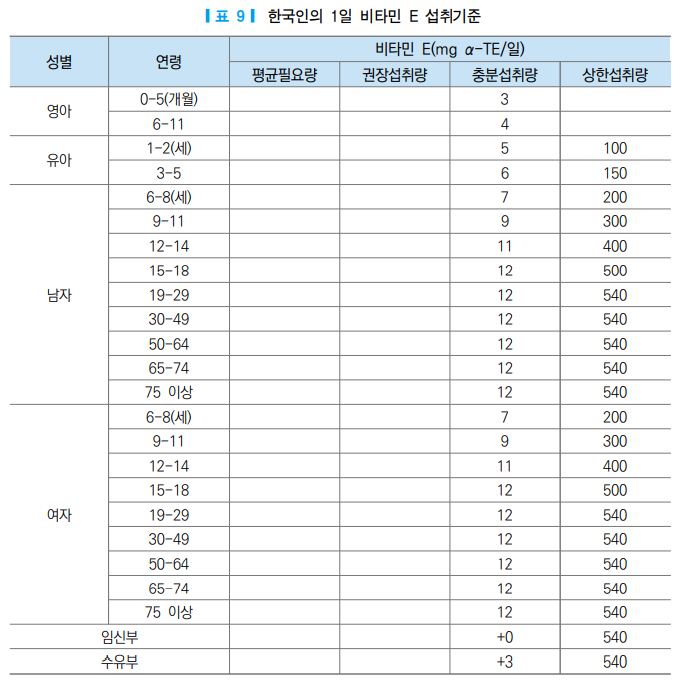
또한 비타민 E의 상한섭취량은 영양소 섭취량이 적절한 일반인을 대상으로 설정된 것이므로 비타민 E와 상호작용을 하는 영양소의 결핍이나 특정 약을 섭취하는 경우에는 상한섭취량 이하로 섭취하더라도 안전 하지 않을 수 있다. 예를 들어 비타민 K의 섭취가 부족하거나 건강상의 문제로 항응고제를 장기간 복용하 는 사람들의 경우 비타민 E 과잉 섭취 시 혈액응고 손상에 대한 위험도에 더 민감하게 반응할 수 있음을 유의해야 한다. 표7 에는 성인의 비타민 E 상한섭취량 설정 근거 및 연령별 상한섭취량이 제시되어 있다.
4 주요 급원식품
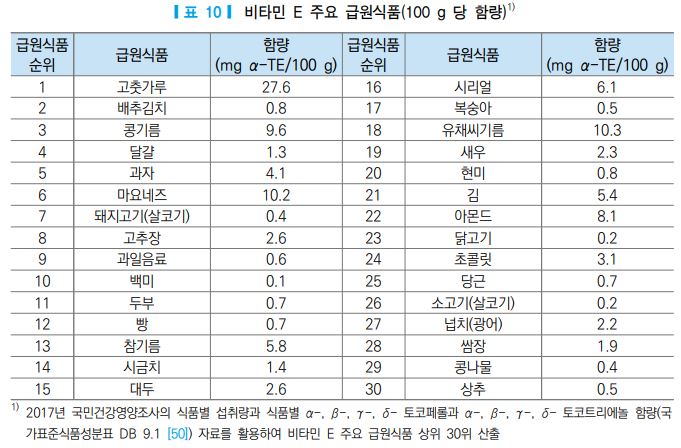
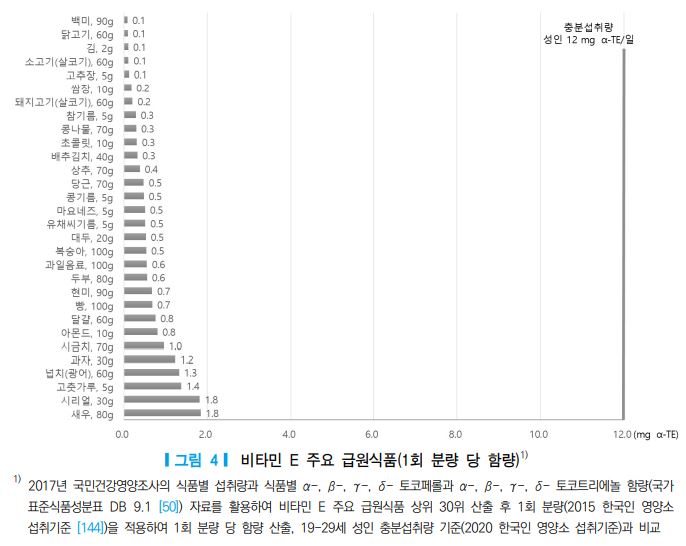
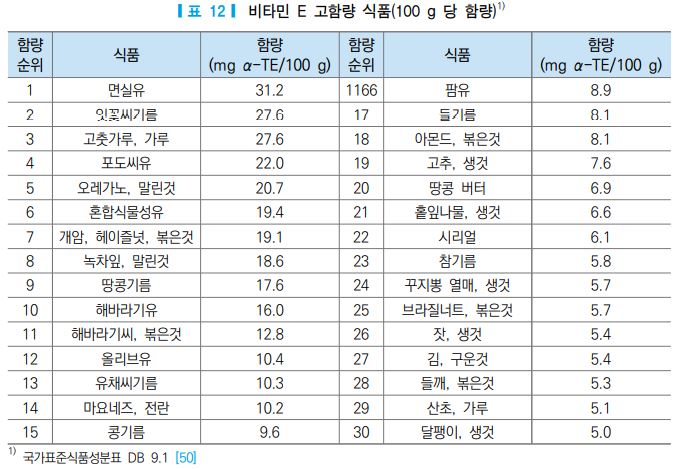
2017년 국민건강영양조사의 식품섭취량 자료를 바탕으로 국가표준식품성분표(농촌진흥청, ver 9.1) [50] 의 α-, β-, γ-, δ- 토코페롤과 α-, β-, γ-, δ- 토코트리에놀 함량의 생체역가를 적용하여 한국인의 비타민 E 주요 급원식품을 산출한 결과, 고춧가루, 배추김치, 콩기름, 달걀, 과자, 마요네즈 순으로 비타민 E 섭취 에 기여하는 것으로 나타났다(표 10). 과자의 경우 미강유나 팜유 등 튀긴 형태가 많으므로 기여식품에 포함된 것으로 생각된다. 이들 급원식품 중 1회 섭취 분량을 기준으로 비타민 E 함량이 가장 높은 식품은 새우, 시리얼, 고춧가루, 광어 순으로 각각 1.8 mg α-TE, 1.8 mg α-TE, 1.4 mg α-TE, 1.3 mg α-TE 이었 으며, 이러한 식품을 1회 분량을 섭취하더라도 성인의 충분섭취량의 약 10-15% 밖에 충족시키지 못함을 알 수 있다(그림 4). 국가표준식품성분표(농촌진흥청, ver 9.1) [50]에서 8가지의 비타민 E 형태의 생체역 가를 적용하여 100 g 당 비타민 E 함량(mg α-TE)이 높은 식품을 살펴보았을 때, 흔히 알고 있는 견과류와 종실류로부터 얻어지는 유지류 외에도 잇꽃씨기름, 오레가노, 헤이즐넛, 녹차잎, 홑잎나물, 꾸지뽕 열매 등 과 같은 식품이 비타민 E를 다량 함유하고 있는 식품인 것으로 나타났다(표 12).
5 향후 2025 섭취기준 개정을 위한 제언
5-1. 섭취기준 설정에서 제기된 문제
비타민 E 권장량을 설정할 때 비타민 E 복합체중에서 활성 비타민으로 간주할 수 있는 비타민의 형태에 대한 적극적인 논의가 필요하며 현재와 같이 α-, β-, γ-, δ-토코페롤, α-, β-, γ-, δ-토코트리에놀의 8가지 형태을 모두 활성 비타민 E로 간주할 경우의 문제점은 아래와 같다.
(1) 한국인 비타민 E 섭취 실태 파악의 부정확성
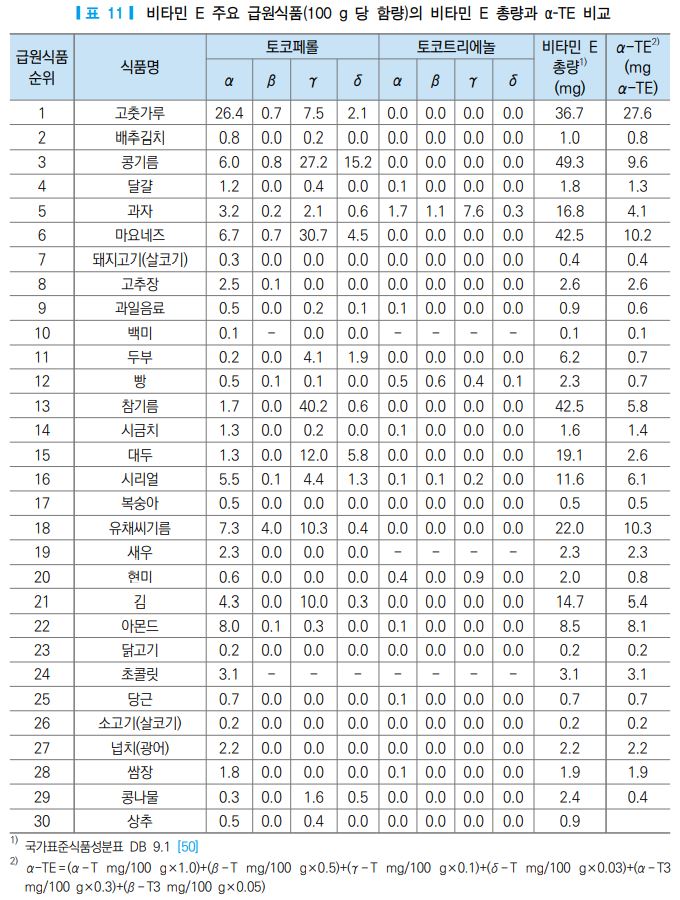
우리나라의 국가표준식품성분표에는 비타민 E의 함량을 α-, β-, γ-, δ-토코페롤, α-, β-, γ-, δ-토코트 리에놀의 총합으로 표시하고 있으며 영양가 계산을 할 때, 이 총합을 권장량 12 mg α-TE의 1일 영양성분 기준치에 대한 비율(%)로 제시하고 있다. 예를 들어, 호박씨 말린 것 100 g을 섭취할 경우, 비타민 E의 총합은(α-토코페롤 1.3 mg, γ-토코페롤 25.4 mg, δ-토코페롤 0.5 mg) 27.1 mg 이며, 생체 역가를 고려 하여 계산하면(α-토코페롤 1.3 mg×1+γ-토코페롤 25.4 mg×0.1+δ-토코페롤 0.5 mg×0.03) 3.9 mg α-TE가 된다. 따라서 호박씨 100 g을 섭취하면 우리나라 비타민 E 권장량인 12 mg α-TE의 32.5%를 만족하는 것이나, 국가표준식품성분표의 섭취식품 영양가 계산에는 1일 비타민 E 영양성분 기준치의 225.8%를 만족 하는 것으로 제시된다.
(2) 국가간 비타민 E 섭취량 비교 불가
미국과 일본에서는 α-토코페롤 수송단백질(α-TTP)의 친화력을 고려하여 권장량 설정을 위한 활성 비타 민 E로 α-토코페롤 만을 이용하고 있으나 우리나라는 α- β-, γ-, δ- 토코페롤(tocopherol)과 α-, β-, γ-, δ- 토코트리에놀(tocotrienol) 을 모두 활성 비타민 E로 간주하고 각 비타민의 생체역가는 동물모델을 이 용한 태아재흡수(fetal resoroption) 실험 결과를 이용하고 있다. 예를 들어 호박씨 100 g을 섭취하면 미국, 일본의 기준에 따르면 1.3 mg(α-토코페롤)의 비타민 E를 섭취한 것이 되고, 우리나라의 기준에 따르면 3.9 mg(α-토코페롤 당량)의 비타민 E를 섭취한 것으로 간주된다.
(3) 비타민 E의 생리적 기능 평가 불가
실질적인 비타민 E 섭취량의 정확한 파악이 선행되지 않은 상태에서 비타민 E 섭취와 만성질환의 연관 성을 평가하는 것은 불가능하다고 할 수 있다.
5-2. 과학적 근거가 부족한 사항
한국인의 비타민 E 섭취실태, 비타민 E 섭취에 따른 혈액의 비타민 E 농도, 정확한 섭취량에 따른 질환 과의 연관성에 대한 모든 연구가 매우 미비한 상태라고 할 수 있다. 이와 같은 연구는 각각의 비타민 E 형태에 따라 개별적으로 정확하게 이루어지는 것이 시급하다 하겠다.
또한 한국 식품의 비타민 E 함유량에 대한 분석 연구도 지속적으로 이루어져야 할 분야라고 할 수 있다.
5-3. 향후 2025 섭취기준 개정을 위해 필요한 과제
1920년대에 비타민 E가 발견된 이후로 항산화기능을 가지는 비타민 E 복합체의 역할에 대한 연구는 지 속적으로 다양하게 이루어지고 있다. 특히 식품을 통한 비타민 E의 섭취는 부정적인 결과를 초래할 수 있 는 보충제를 통한 비타민 E와 다르게 심순환계질환, 암, 중추신경계질환 등 만성질환의 위험성을 낮추어 주는 것으로 일관되게 보고되고 있다. 따라서 식품을 통한 비타민 E 섭취 실태의 정확한 평가는 비타민 E 관련 연구의 시발점이라 할 수 있으며, 향후 2025 비타민 E 섭취기준 개정을 위한 시급한 과제를 제시하 면 다음과 같다.
(1) 한국인의 비타민 E 섭취 실태의 정확한 파악
한국인의 비타민 E 복합체 섭취 실태에 대하여 우선적으로 α-, β-, γ-, δ-토코페롤, α-, β-, γ-, δ-토코 트리에놀의 개별적 섭취량 산출이 필요하며, 이를 통하여 한국인의 총 비타민 E 섭취량 중 α-토코페롤의 기여도 파악이 시급하다.
(2) 각각의 비타민 E 섭취와 그에 따른 혈액의 농도 변화 평가
또한 α-, β-, γ-, δ-토코페롤, α-, β-, γ-, δ-토코트리에놀의 개별적 섭취량과 이에 따른 각 비타민 E의 혈액 농도와의 연관성에 대한 평가가 필요하다 하겠다.
(3) 우리나라 상용 식품의 비타민 E 함유량 평가
우리나라 상용식품의 비타민 E 복합체 분석을 통한 데이터베이스 구축은 지속적으로 노력을 기울여야 할 분야라고 할 수 있다.
(4) 우리나라 국민의 비타민 E 첨가식품 및 보충제 섭취 실태 평가
비타민 E의 첨가식품 및 보충제 섭취 현황은 권장량 설정에 필수적인 자료일 뿐 만 아니라 α-토코페롤 이성질체의 활성을 예측하는 자료로도 활용될 수 있다. 특히 2016년부터 미국에서는 RRR α-토코페롤과 all-rac α-토코페롤의 비율을 1.63:1에서 2:1로 조정하였으므로 이와 연관하여 우리나라 국민의 섭취실태에 대한 재평가도 시급한 과제중의 하나라고 할 수 있다.
2020 한국인 영양소 섭취기준(지용성비타민-비타민E)
👉
5년 단위로 발행 됨.
'2020 한국인 영양소 섭취기준' 전체보기
http://www.mohw.go.kr/react/jb/sjb030301vw.jsp?PAR_MENU_ID=03&MENU_ID=032901&CONT_SEQ=362385
'식품공부 > 영양소' 카테고리의 다른 글
| 수용성비타민/비타민C-2020 한국인 영양소 섭취기준 (1) | 2022.11.18 |
|---|---|
| 지용성비타민/비타민K-2020 한국인 영양소 섭취기준 (1) | 2022.11.18 |
| 지용성비타민, 비타민D-2020 한국인 영양소 섭취기준 (1) | 2022.11.17 |
| 지용성비타민,비타민A-2020 한국인 영양소 섭취기준 (1) | 2022.11.17 |
| 다량무기질,칼슘Ca-2020 한국인 영양소 섭취기준 (0) | 2022.11.16 |



